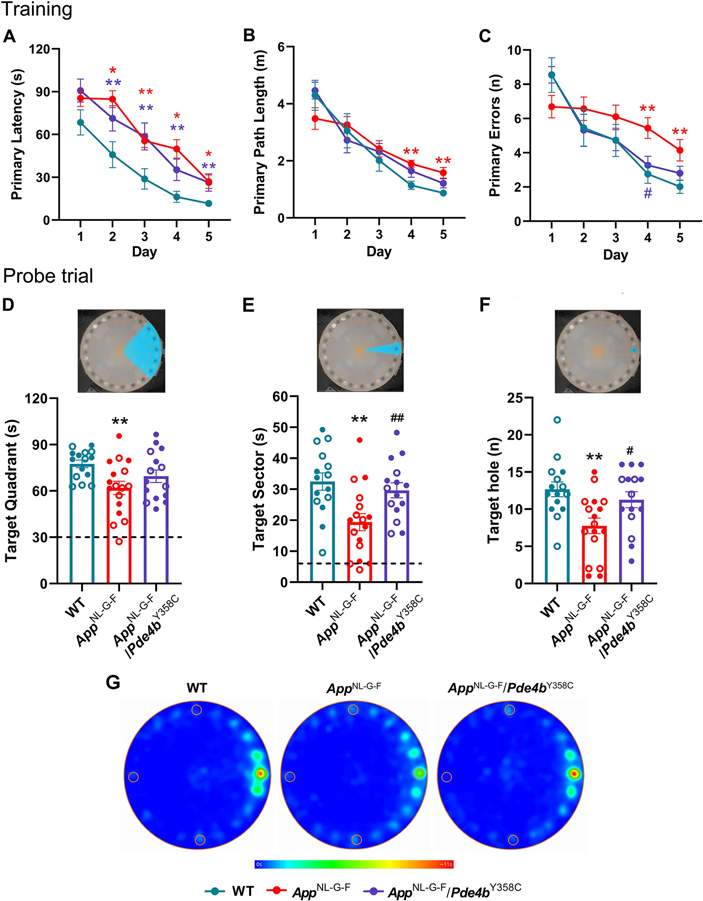

Рис. 3. «Двойные мутанты» (AppNL-G-F/Pde4bY358C, фиолетовый цвет) лишь незначительно отличаются от здоровых мышей дикого типа (WT, бирюзовый цвет) по показателям длины пути, числа ошибок и попаданий мордочкой в ложные лунки в лабиринте Барнса, в отличие от обычных «альцгеймеровских» мышей (AppNL-G-F, красный цвет). A — первичная задержка (время от начала испытания до первого достижения мышью убежища), B — длина пройденного пути, C — количество ошибок, D, E, F — время, проведенное мышью в области, обозначенной голубым цветом, G — тепловые карты, показывающие, сколько раз мышь сунула мордочку в ту или иную лунку. Рисунок из обсуждаемой статьи
Позитронно-эмиссионная томография выявила дополнительные обнадеживающие признаки у «двойных мутантов»: у них не снижалась скорость метаболизма глюкозы в мозге. Это снижение — один из первых и грозных признаков болезни Альцгеймера, появляющийся раньше ощутимых структурных изменений мозга и даже до развития симптомов. Обычные «альцгеймеровские» мыши его демонстрировали, а вот мыши, которым дополнительно выключили фосфодиэстеразу — нет. На снимках ПЭТ их мозг «светился» лишь чуть менее ярко, чем у контрольной группы дикого типа (рис. 4).
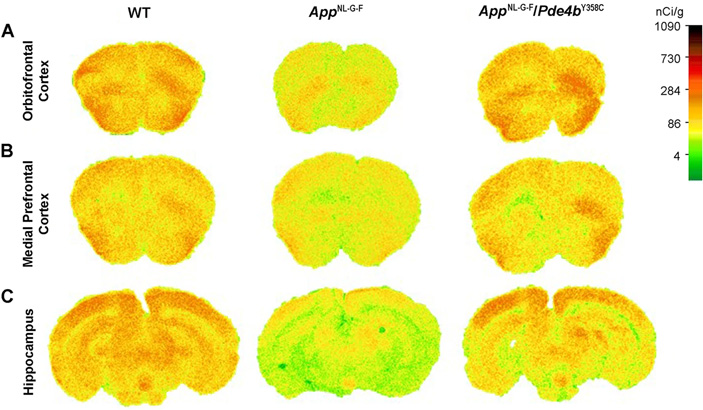

Рис. 4. Позитронно-эмиссионные томограммы (ПЭТ) различных отделов мозга мышей из трех участвовавших в экспериментах групп, показывающие уровень метаболизма глюкозы. Чем «теплее» цвет, тем интенсивнее мозг метаболизирует глюкозу. WT — дикий тип, AppNL-G-F — «альцгеймеровские» мыши, AppNL-G-F/Pde4bY358C — «двойные мутанты». Заметно, что у «двойных мутантов» снижение метаболизма глюкозы незначительно по сравнению с обычным и «альцгеймеровскими» мышами. Рисунок из обсуждаемой статьи
К сожалению, все мыши были убиты в ходе эксперимента. Это было необходимо, чтобы оценить интенсивность воспаления в их мозге — для этого мозг гомогенизируют до состояния жидкой кашицы и измеряют в этой кашице уровень определенных белков, маркеров воспаления. У двойных мутантов он также оказался ниже, чем у обычных «альцгеймеровских» мышей. Получается, что «отключение» гена фосфодиэстеразы резко смягчает симптомы болезни Альцгеймера и улучшает метаболизм клеток мозга, несмотря на продолжающееся отложение амилоида. Так может, и новые лекарства должны быть направлены вовсе не на него?
Это исследование стало еще одним доказательством, что блокирование фосфодиэстеразы 4B может помочь пациентам с болезнью Альцгеймера. Исследователи активно накапливают свидетельства в пользу этого в последние годы. В частности, было показано, что имеющиеся ингибиторы фосфодиэстеразы могут замедлять прогрессирование болезни Альцгеймера у мышей и человека (J. Sheng et al., 2022. Inhibition of phosphodiesterase: A novel therapeutic target for the treatment of mild cognitive impairment and Alzheimer’s disease), а у пациентов с этой болезнью нарушена внутриклеточная сигнализация через цАМФ и цГМФ (O. Sanders, L. Rajagopal, 2020. Phosphodiesterase Inhibitors for Alzheimer’s Disease: A Systematic Review of Clinical Trials and Epidemiology with a Mechanistic Rationale). Пока до конца не ясно, как именно фосфодиэстераза 4B связана с гибелью нейронов при болезни Альцгеймера, но все предложенные механизмы связаны с ее биохимической функцией по расщеплению цАМФ и цГМФ. А значит, если заблокировать этот фермент каким-нибудь специфичным ингибитором, эффект будет такой же, как и от его генетического выключения. Такие ингибиторы ученые уже ищут — благо фосфодиэстеразы можно блокировать флавоноидами, кофеином, капсаицином (жгучим веществом перца), ресвератролом (антиоксидантом из красного вина) и антидепрессантом ролипрамом. Однако, прежде чем такой метод будет исследован на людях, на основе этих веществ нужно создать именно специфичный ингибитор — имеющиеся соединения блокируют сразу несколько подтипов фосфодиэстераз, приводя к побочным эффектам.
Как только такой ингибитор будет создан, новая надежда появится не только у пациентов с болезнью Альцгеймера — исследователи надеются применить его у пациентов с болезнью Хантингтона, другим нейродегенеративным заболеванием. Но даже если и эта попытка окажется неудачной, серия исследований по фосфодиэстеразе 4Β имеет все шансы оказаться переворотом в исследовании болезни Альцгеймера. Ведь обсуждаемая работа наглядно показала, что болезнь можно затормозить, никак не влияя на отложения амилоида. Амилоидную теорию по-прежнему рано списывать со счетов — но, возможно, стоит окончательно перестать гоняться за амилоидом при разработке лекарств от болезни Альцгеймера, сосредоточившись на других мишенях.
Источник: Paul Armstrong, Hüseyin Güngör, Pariya Anongjanya, Clare Tweedy, Edward Parkin, Jamie Johnston, Ian M. Carr, Neil Dawson & Steven J. Clapcote. Protective effect of PDE4B subtype-specific inhibition in an App knock-in mouse model for Alzheimer’s disease // Neuropsychopharmacology. 2024. DOI: 10.1038/s41386-024-01852-z.
Георгий Куракин
